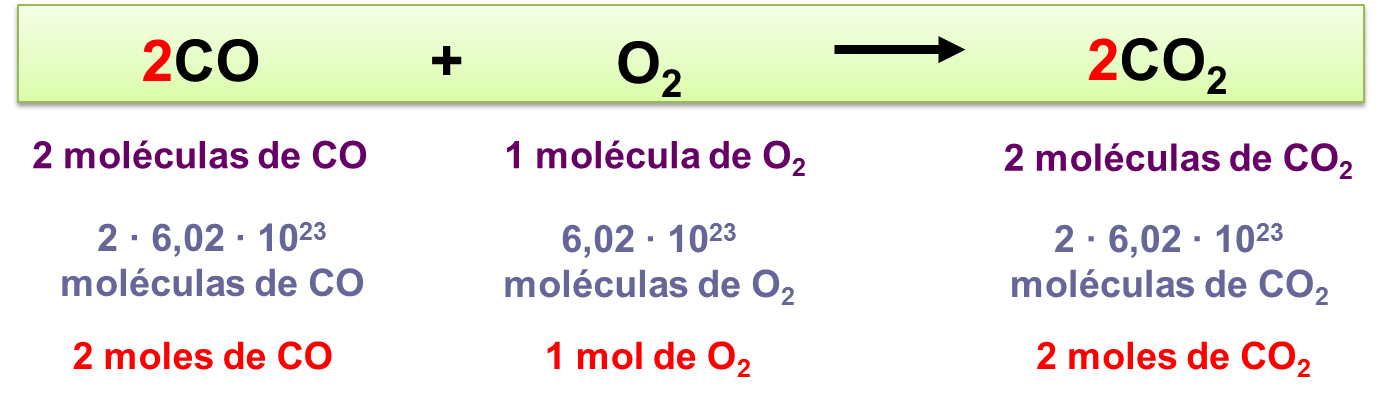
Suma De Coeficientes Estequiometricos
Qué coeficiente hace falta para balancear la siguiente ecuación c2h6o o2 2 co2 3 h2o investigue sobre los gases y aguas residuales que producen las industrias y redacte un ensayo de 100palabras en una taza hay dos cucharadas de azúcar cuya masa es de 4 8g y media cucharada de café cuya masa es de 0 7g cual es el porcentaje en masa del café.
Suma de coeficientes estequiometricos. En caso de que no ser asi este se multiplica por una constante entera positiva y asi sucesivamente con todos los términos hasta encontrar la. B 1 átomo de ba 2 átomos de o. C se resuelve el sistema. Por lo tanto 8x 20y representa la suma de los coeficientes de la expresión 3x 9y 5x 11y.
A la suma de los coeficientes estequiométricos es 27. Coeficiente e quantidade de substância mol vamos agora obter a proporção em mols através dos coeficientes estequiométricos. En primer lugar pon los coeficientes de x juntos. P 5516 obtención de anilina a partir de nitrobenceno y ditionito de sodio p 5363 comprobación de la ley de conservación de la masa y ajuste redox p 5351 suma de coeficientes estequiométricos y agente oxidante p 735 diagrama de pila y potencial estándar p 729 ajuste método ión electrón medio básico.
Encuentra la suma de los coeficientes de 3x 9y 5x 11y. Calcula la suma de coeficientes estequiometricos en la reaccion. Al balancear la ecuación. Si como en el ejemplo el número de coeficientes es superior en una unidad al de elementos entonces se iguala cualquiera de ellos a uno.
Escribimos las semirreacciones de oxidación y reducción ajustadas. N2 h2 nh3 la suma de los coeficientes estequiométricos es. 3 5 8. El balanceo de ecuaciones químicas implica que todos los elementos presentes en dicha ecuación tienen el mismo número de átomos a cada lado.
3 ver otras preguntas de exámenes nacionales. Si una vez resuelto el sistema los coeficientes resultantes fueran fraccionarios se convierten en enteros multiplicando todos ellos por su mínimo común denominador. Si se tiene un carbono del lado derecho tiene que haber uno del lado izquierdo. Son los subíndices que se ubican al lado derecho de un átomo o un ion e indican la cantidad de átomos o iones que tiene la especie.
Exámenes nacionales 17 06 2019 13 00 4269976 cuántas moles de h2o se producirán en una reacción donde se consumen completamente 3 25 moles de o2 suponiendo que se tiene hidrógeno en. Pon las ecuaciones juntas de nuevo con las sumas. 1 n2 g 3 h2 g 2 nh3 g ver resposta. A 1 átomo de na 1 átomo de o 1 átomo de h.
C3h12 o2 co2 h2o pide más detalles. 9 11 20. A continuación pon los coeficientes de y juntos.